发布时间:2025/03/27 点击数:52
发布时间:2025/03/27 点击数:52 寡核苷酸疗法的兴起,用以人为本的方法克服ADMET开发挑战
一、前言:探索未知的奇妙之旅
前沿新模式药物或advanced therapy是指超越传统小分子方法的创新方法,能够更准确、更有效地针对疾病。

它们旨在治疗难以用传统疗法治疗且可能被归类为“无药可用”的复杂疾病和病症。根据BCG 的《2024 年新药模式报告》[1],新模式在制药/生物技术预计管线价值中占 1680 亿美元,比 2023 年增长14%。到2029年,分析师预测排名前 10 位的药物中将有 9 种是新模式。尽管抗体占后期临床前管线的大部分,但在早期阶段可以发现许多其他模式,包括更适合细胞内靶点的寡核苷酸。
然而,寡核苷酸具有独特的开发挑战,需要适应临床前测试工作流程。一个主要的挑战与体内测试有关。由于人类和非人类灵长类动物 (NHP) 之间的核酸碱基序列高度保守,因此它们被较广使用,但价格昂贵。然而,即使是 NHP 也可能错误地预测人类反应——正如 2006 年单克隆抗体 TGN1412 的 1 期临床试验所证明的那样。由于恒河猴 CD4+ 效应记忆 T 细胞缺乏 CD28 表达,六名健康志愿者患上了危及生命的疾病(Eastwood等人, 2010)[2]。因此,在体内研究之前确保您对寡核苷酸的递送、安全性和有效性有尽可能多的信心,有利于很大限度地降低风险。
为了实现这一目标,临床前工具箱需要现代化,以变得更加以人为本。新方法 (NAM),包括器官芯片 (OOC),为解决许多发展挑战提供了可行的途径。而且,随着 FDA 现代化法案 2.0 于 2022 年通过,监管机构支持在适当情况下使用新方法代替动物试验来评估药物的安全性和有效性。
在本系列中,我们首先探讨了为什么基于寡核苷酸的疗法越来越受欢迎,它们的 ADMET 发现和开发挑战,以及体外人类 OOC 模型如何通过提供数据丰富的见解来帮助规避这些问题,下一期我们将用2个分别与葛兰素史克公司 (GSK) 、阿斯利康(AstraZeneca)合作的器官芯片案例来说明,OOC在该领域的突出益处,从而更好地支持或证明体内非人灵长类(NHP)或人体研究的费用合理性问题。
二、为何基于寡核苷酸的疗法越来越受欢迎?
基于寡核苷酸的疗法或基于RNA的疗法是干扰特定 RNA 的短寡核苷酸序列。它们包括反义寡核苷酸 (ASO)、RNA 干扰 (RNAi)、小干扰 RNA (siRNA)、microRNA (miRNA) 和适配体(aptamers)。人们对寡核苷酸治疗的兴趣源于对人类基因组的深入理解及其与多种疾病的遗传关联。此外,与传统小分子药物相比,寡核苷酸类药物的研发过程相对较快,并且对各类规模的机构都具有较高的可及性。
1998 年至 2024 年期间,约有 18 种基于寡核苷酸的疗法获得了市场批准(请查看文末附表2)。近年来,寡核苷酸类治疗取得了重要进展,其中一个关键因素是递送系统的应用,如脂质纳米颗粒(LNPs)和N-乙酰半乳糖胺(GalNAc)偶联技术,使药物能够靶向肝脏用于治疗肝脏疾病。例如,2016年,治疗转甲状腺素淀粉样变性(ATTR)的Patisiran(商品名Onpattro)采用LNPs递送siRNA至肝脏。2019年,利用GalNAc偶联技术靶向肝脏的Givosiran(商品名Givlaari)获批用于急性肝卟啉病(一组罕见的遗传性代谢疾病)的治疗。
利用糖分子GalNAc进行肝脏靶向治疗的机制依赖于无唾液酸糖蛋白受体(ASGPR),该受体主要存在于肝细胞表面。GalNAc偶联的寡核苷酸能够高亲和力结合ASGPR,并通过内吞作用迅速从全身循环中清除。一旦进入细胞,治疗性寡核苷酸便从受体中释放,并通过靶向特定信使RNA(mRNA)序列发挥治疗作用。这一策略不仅提高了药物的效力和有效性,使其在更低剂量下即可发挥作用,还减少了非靶向效应,并可能延长给药间隔,同时降低免疫原性。随着研究和开发的持续推进,基于GalNAc的疗法在治疗遗传疾病、代谢疾病以及传染病等多种疾病方面展现出巨大的未来潜力。
2021年,诺和诺德(Novo Nordisk)收购了Dicerna,以充分利用这一领域的潜力。随后,2023年《Bioprocess International》的一篇报道引用了诺和诺德研究与早期开发执行副总裁Marcus Schindler的话,他表示:“目前我的管线中相当大一部分是寡核苷酸类药物。” 他解释说,原因在于“构建一个工具箱,以加速我们在药物发现方面的工作。”
关于诺和诺德如何支持寡核苷酸药物的开发,他进一步指出:“首先,我们采用了一种以人为本的方式来理解复杂的生物学机制。我们的研究始于能够模拟我们关注的物种——即人类的数据集和实验模型。”
那么,为什么这一类药物需要更加以人为中心的研究方法?在其发现和开发过程中,又存在哪些挑战,使得我们需要重新思考前临床研究工具箱的构建?
三、寡核苷酸治疗肝病的ADMET挑战
寡核苷酸类药物的吸收(Absorption)、分布(Distribution)、代谢(Metabolism)、排泄(Excretion)和毒理学(Toxicology,简称ADMET)方面的挑战与前述观点密切相关。寡核苷酸不同于传统小分子化合物,而动物也并非人类。
寡核苷酸可通过多种机制发挥其预期的药理作用,但较常见的方式是利用互补的核苷酸碱基序列,与细胞内核酸的靶向序列结合。其中,一些寡核苷酸可能对人类高度特异,因此在研究中不得不使用非人灵长类(NHP),甚至在某些情况下无法使用其他非人动物物种。测试物种活性替代性寡核苷酸(surrogate oligonucleotides)是一种解决方案,但这并不能改变动物并非人类这一根本事实。
计算模拟(in silico)和体外实验(in vitro)方法可用于识别潜在的脱靶杂交效应(off-target hybridization effects),但这些方法各有局限性:
• 体外模型的生理相关性有限(这一点将在后文详细探讨);
• 计算模型的准确性则取决于输入数据的质量和完整性。
在肝病的寡核苷酸治疗开发及其前临床ADMET评估过程中,仍然存在诸多挑战。下表(表1)总结了其中非常关键的问题。
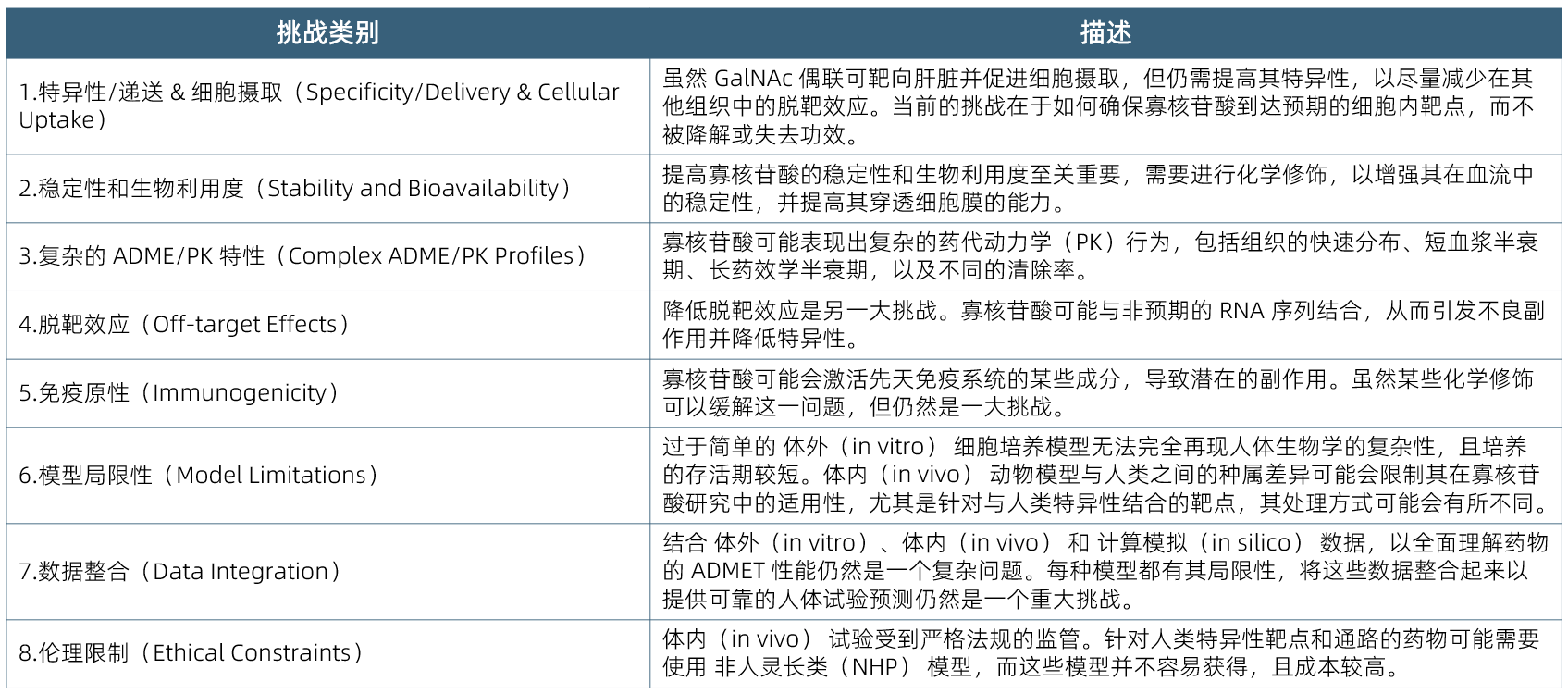
表1:寡核苷酸治疗的ADMET分析关键挑战
四、器官芯片模型如何促进寡核苷酸疗法在肝病 ADMET 研究中的进展
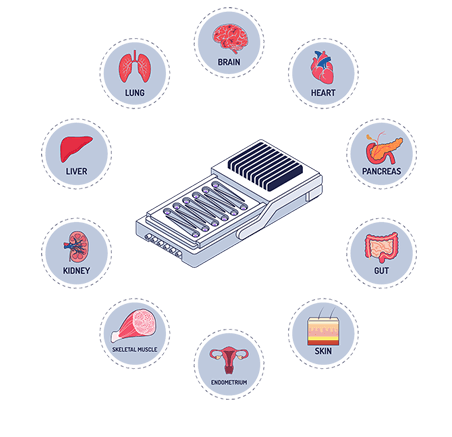
上述挑战凸显了创新方法(如 OOC(器官芯片,Organ-on-a-Chip))在提高寡核苷酸药物临床前测试预测能力方面的重要性。OOC,又称为 微生理系统(MPS,Microphysiological Systems),将构建特定器官级响应的功能性组织所需的技术整合到微型化的系统中。
为了模拟肝脏环境,OOC 模型通常使用人原代肝细胞(PHHs,Primary Human Hepatocytes),并根据需要加入肝脏驻留免疫细胞(如 库普弗细胞(Kupffer cells))培养形成 3D 微组织,并在专门设计的支架中进行培养。这些微组织通过培养基持续灌流以模拟血流环境,从而提供气体交换和营养输送。这种动态 3D 微环境使得肝细胞的存活和功能维持数周(通过白蛋白和乳酸脱氢酶水平进行量化),相比之下,传统 2D 体外肝细胞培养仅能维持几天。
OOC旨在克服传统临床前模型的局限性,提高人体生理相关性,并支持动物模型的合理使用。它帮助研究人员仅推进更具潜力的候选药物进入后续试验,同时在缺乏药理学相关模型的情况下,提供更有价值的决策依据。
1、OOC 模型如何应对 ADMET 挑战?
(1)长期培养能力
• 相较于静态 PHH 细胞培养,OOC 细胞培养体系的 长寿命 使得 寡核苷酸浓度效应 可被准确测量。
• 通过对 肝微组织给药 并随时间测量 寡核苷酸摄取及基因敲低效应,可以更好地评估其作用。
• 由于基因敲低效应通常需要 较长时间才能显现,OOC 的 长期培养特性 能提供更准确的结果。
(2)重复给药实验
• 由于 OOC 系统可长期维持细胞功能,因此研究人员可以 进行多次寡核苷酸给药,以优化 用药策略,从而在进入 体内动物实验或首.次人体试验(FIH,First-in-Human) 前获得关键数据。
(3)监测免疫细胞活化及安全性评估
• Liver-on-a-chip(肝芯片) 系统可在整个实验过程中 动态监测肝细胞健康状况,识别 潜在不良反应,例如 先天免疫细胞活化 等毒性效应。
(4)优化计算模拟(in silico)预测能力
• 人体相关数据 可作为输入信息,优化 计算机模拟模型(in silico models),提高药物 ADMET 预测的准确性。
2、Liver-on-a-chip 在 ADMET 研究中的应用
美国FDA已认可肝芯片在小分子药物代谢、蓄积及毒性测试方面优于传统方法[3]。目前,制药及生物技术公司正在通过英国CN Bio PhysioMimix OOC 或CRO合同研究服务[4],探索其在 寡核苷酸疗法ADMET研究中的应用潜力。
下一期我们将用近期的2个分别与葛兰素史克公司 (GSK) 、阿斯利康(AstraZeneca)合作的器官芯片案例,来说明,OOC在该领域的突出益处,从而更好地支持或证明体内非人灵长类(NHP)或人体研究的费用合理性问题,敬请关注。
[1]https://www.bcg.com/publications/2024/new-drug-modalities-report
[2]https://bpspubs.onlinelibrary.wiley.com/doi/10.1111/j.1476-5381.2010.00922.x
[3]https://ascpt.onlinelibrary.wiley.com/doi/10.1111/cts.12969
[4]https://cn-bio.com/physiomimix-ooc/
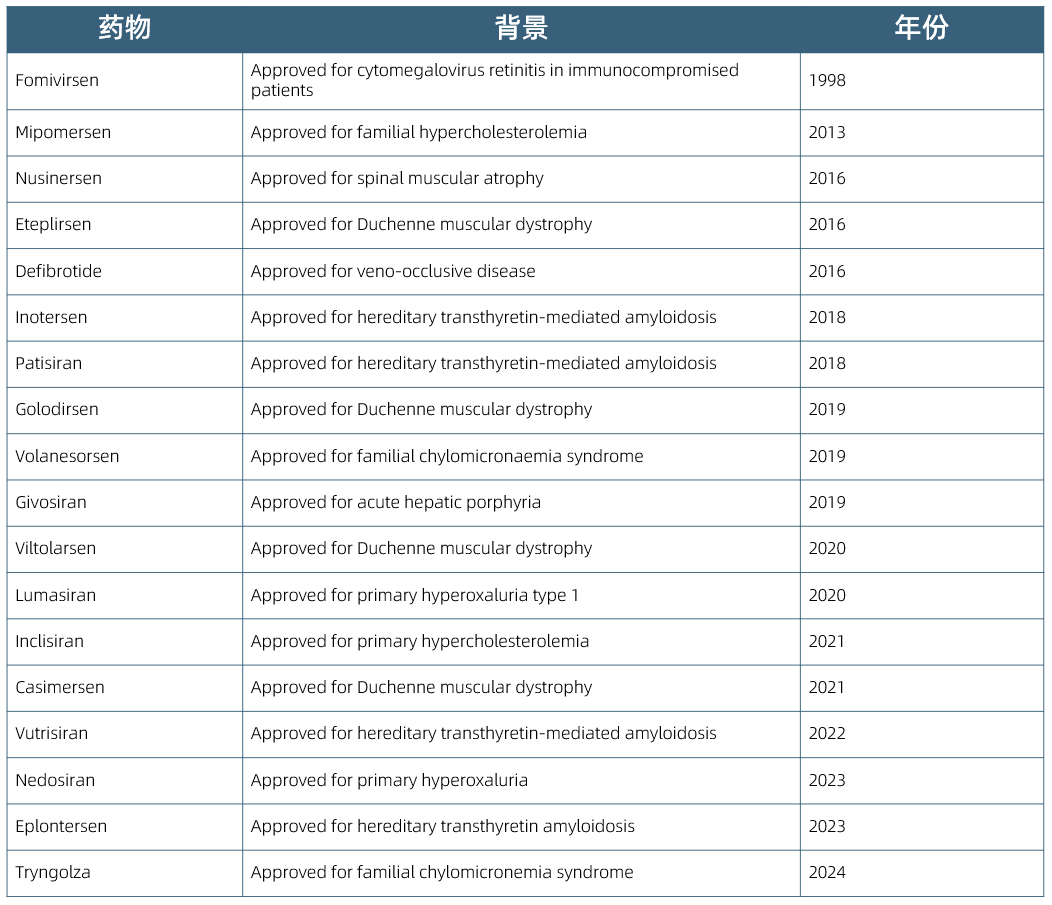
表2:1998年至2024年美国食品药品监督管理局批准的寡核苷酸疗法
本文由曼博生物翻译编辑整理,原文参考CN Bio官网。上海曼博生物医药科技有限公司是CN Bio正式授权的代理商,如有需要或支持请联系我们。